SALICILATO DE METILO
O Salicilato de Metilo (Methyl Salicylate, nome INCI: methyl 2-hydroxybenzoate) é o éster de álcool metílico e ácido salicílico. De acordo com diversos estudos, o ácido salicílico é o principal produto metabólico do Salicilato de Metilo por hidrólise.
Em cosméticos e produtos de higiene pessoal, o Salicilato de Metilo é utilizado como desnaturante, aromatizante, higiene oral, agente perfumante e calmante. É utilizado como ingrediente em diversas misturas de fragrâncias e como aromatizante e calmante em produtos de higiene oral. O Salicilato de Metilo não se encontra atualmente incluído nos anexos do Regulamento Europeu de Cosméticos (nº 1223/2009), o que significa que o seu uso não tem restrições em produtos cosméticos.
Em 2019, o Comité Europeu de Avaliação de Risco (RAC – European Risk Assessment Committee) da Agência Europeia de Produtos Químicos (ECHA – European Chemicals Agency) emitiu um parecer sobre o Salicilato de Metilo, recomendando uma classificação como “Tóxico para a reprodução da categoria 2” e “Sensibilizante cutâneo da categoria 1B” para este ingrediente, com base numa comparação com os dados disponíveis sobre o ácido salicílico. Na sequência do parecer do RAC, é esperada uma alteração ao Anexo VI do Regulamento CLP (Regulamento (CE) 1272/2008 relativo à classificação, rotulagem e embalagem de substâncias e misturas).
De acordo com o Regulamento de Cosméticos da UE, o uso de substâncias classificadas como CMR (cancerígenas, mutagénicas ou tóxicas para a reprodução) deve ser proibido em produtos cosméticos, a menos que, a excepcionalmente, condições específicas sejam cumpridas. Uma substância CMR classificada na categoria 2 poderá ser utilizada em produtos cosméticos se a mesma fori avaliada pelo Comité Científico de Segurança do Consumidor da Comissão Europeia (SCCS – Scientific Committee on Consumer Safety) e considerada segura para utilização em produtos cosméticos.
Considerando a opinião do RAC e a classificação esperada do Salicilato de Metilo como “Tóxico para a reprodução, categoria 2”, um dossiê foi enviado pela Cosmetics Europe para apoiar a segurança do Salicilato de Metilo. A Comissão solicitou ao SCCS a realização de uma avaliação de segurança do ingrediente, tendo em conta o dossiê apresentado e também a concentração máxima deste ingrediente que é utilizada nas diferentes categorias de produtos cosméticos.
OPINIÃO FINAL DO SCCS SOBRE O SALICILATO DE METILO
No mês passado, o SCCS emitiu o seu parecer final sobre o Salicilato de Metilo. Este ingrediente deve ser considerado um sensibilizante fraco cutâneo (em humanos) e irritante para os olhos.
O SCCS concluiu que o Salicilato de Metilo é considerado seguro quando usado em cosméticos até à concentração máxima fornecida no dossiê apresentado (apresentada na tabela abaixo).
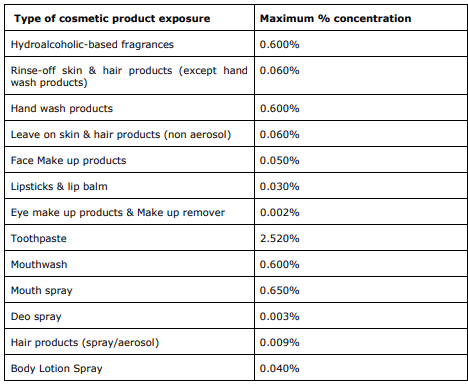
O SCCS também expressou algumas preocupações relativamente ao uso deste ingrediente em cosméticos. Como o Salicilato de Metilo pode ser usado em produtos de consumo que não sejam cosméticos (por exemplo, produtos de limpeza doméstica, produtos de tratamento do ar, biocidas, ceras, etc.), pode aumentar a dose de exposição sistémica com a possibilidade de exceder o nível considerado seguro. Além disso, o Salicilato de Metilo é metabolizado em ácido salícilico (também classificado como tóxico para a reprodução, usado em cosméticos e considerado seguro nas condições estabelecidas no parecer SCCS/1601/18) no corpo e, portanto, a exposição combinada a produtos cosméticos que contenham os salicilatos podem aumentar a dose de exposição sistémica, com a possibilidade de exceder o nível seguro.
Como o óleo de wintergreen (gaultéria) pode conter até 99% de Salicilato de Metilo, o cálculo do teor de Salicilato de Metilo num cosmético deve considerar qualquer fração proveniente deste óleo.
Se desejar obter mais informações sobre a segurança de ingredientes cosméticos, não hesite em contatar-nos através de info@criticalcatalyst.com.
Referências:
- Regulation (EC) No 1223/2009 of the European Parliament and of the Council of 30 November 2009 on cosmetic products.
- Scientific Committee on Consumer Safety (SCCS). Opinion on Methyl salicylate (methyl 2-hydroxybenzoate). SCCS/1633/21. 2021
- Scientific Committee on Consumer Safety (SCCS). Opinion on Salicylic acid (CAS 69-72-7). Submission I. SCCS/1601/18. 2019














